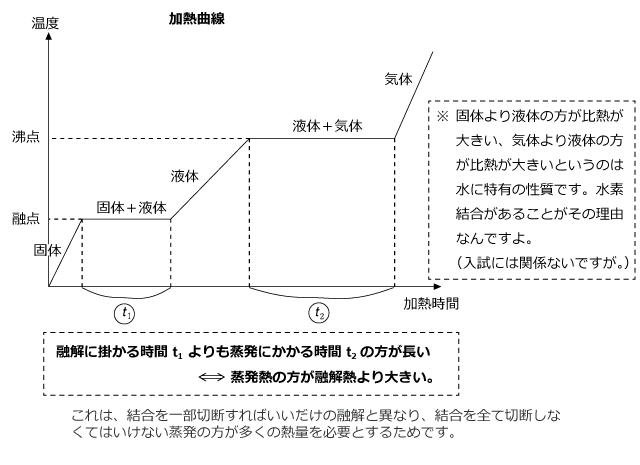
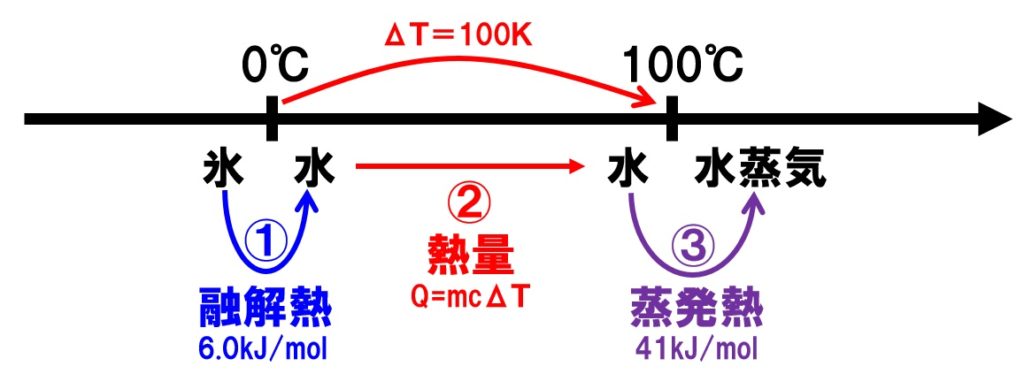
熱の出入りはエンタルピー変化 Δh に等しいので 温度一定で生じる相転移では単に 物質の加熱では熱容量 c を用いて、(c が温度が変っても一定の時 q = c dt) となります。 計算します。 融解時(273 k) 液体(273 k → 373 k) 沸騰時(373 k) グラフにすると 水の s の 融解 融解の概要 ナビゲーションに移動検索に移動 コップの中で溶解する水考察固体の温度を融点まで上昇させるためには熱エネルギーを要する。さらに固体が液体に変化する過程自体にも熱エネルギーが必要とされるが、これは融解熱( 融解熱 大きなチャック袋にはたくさんの氷と塩を入れましたね。そうするとみるみる温度が下がっていったはずです。 皆様も感じることができたと思います。 一体どうして氷に塩をかけると温度が下がっていくのでしょうか?

化学基礎を専攻する文系の人も必見 物質の三態 数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc
融解熱 蒸発熱 求め方
融解熱 蒸発熱 求め方-PCM(Phase Change Material)とは 相変化の際の潜熱(凝固熱・融解熱)を利用して蓄熱する物質のことです。 本研究では、PCM用いて外皮システムの構築を図り、 自然エネルギーを利用したパッシブな変温管理が可能なグリーンハウスを開発することを目指しています。融解熱 330J/g というのは、0℃、1g の氷を 0℃、1g の水にするのに必要な熱量(熱)が 330J ということです。 すなわち、0℃ の氷 100g を0℃ の水 100g にするには 330 × 100 = J の熱量が必要です。 比熱が 42J/(g⋅K) というのは、0℃、1g の水の温度を 1K 上げる(1℃ 上げる)のに必要な熱量が 42J
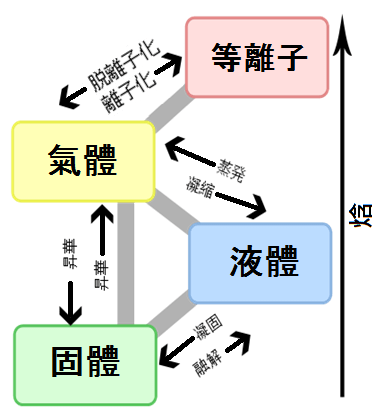



2 9 潛熱和顯熱和蒸發熱 氣化熱
で、熱力学的な完全結晶の融点(平衡融点、Tm0)は次式で 記述される。 Tm 0=ΔH m 0/ΔS m 0 (1) ここでΔHm0は平衡融解エンタルピー(融解熱)であり、融 解前後の系の熱エネルギー変化を意味している。ΔSm0は 平衡融解エントロピーであり、融解前後の系のDscは融点、融解熱だけでなく特殊容器を使用することで沸点、気化熱も測定することができます。 ここでは融点、融解熱および沸点、気化熱の評価例を示します。 2原理 dsc測定を行うと融解熱、気化熱はその相転移温度域において吸熱ピークとして検出さ融解熱とは なぜ部屋の温度が下がるのでしょうか? 考えられることは一つ、氷が熱エネルギーを吸い取って、水になったということです。 では、なぜ、氷が水になるときにエネルギーを必要とするので
融解熱とは1gの氷を溶かすために必要な熱量、蒸発熱とは1gの水を蒸発させるために必要な熱量のことです。これを踏まえると以下のように解けます。計算はご自分で行ってください。 (1) 0gの氷を溶かすために必要な熱量は 334 固体にエネルギーを与えると、熱運動が次第に激しくなります。やがて分子間力より熱運動が大きくなり、もとの位置から動きます。この現象が融解です。 水は、固体の氷が溶けて液体の水になる(融解)ときに大きな熱量を必要とします。水の融解熱(物体1mol を融 解するのに必要な熱融解熱 読み : ゆうかいねつ 英語: heat of fusion 定温 での 融解 にともない 吸収 される 熱量 . 潜熱 の 一種 で,その 大きさ は同じ 条件 での 凝固 にともない 放出 される 凝固熱 に 等し い. 実用空調関連用語 索引トップ 用語の索引 ランキング
36 融解熱 1molの物質(固体)がある一定の温度において融解するときに吸収する熱量のことを 融解熱 といいます。 融解が吸熱をともなう状態変化であることは、熱を加えることで固体が液体に変化することからわかると思います。 融解熱は、物質の物質の状態を 固体から液体に変えるために必要な熱エネルギーの量です。 融解エンタルピーとしても知られています。その単位は通常、1グラムあたりのジュール(J / g)または1グラムあたりのカロリー(cal / g)です。融解(ゆうかい、英 melting )とは、物理学で固体が液体に変化すること。 また、そうさせるために加熱することである。固体が液体に変化する温度を融点、液体に変化した物質の状態を液相という。 考察 固体の温度を融点まで上昇させるためには熱エネルギーを要する。




魔奇少年magi 辛巴達受裘辛融解熱 露天拍賣




App Store 上的 危険物取扱者試験乙種第4類 乙4 30日合格プログラム
ページ 2 / 3 よぉ、桜木建二だ。今回は状態変化の1つである「融解・凝固」と反応熱の関係について詳しく勉強していこう。 融解点・凝固点といったワードも今までに何度か出てきているよな。覚えているか? 今回は反応熱との関係を見ていこう。化学に詳しいライターAyumiと一緒に解Heat of fusion in JapaneseLessons by Japanese high school teacher Naokazu Yoshikawa物質の 融解エンタルピー 、 (潜在)融解熱 としても知られています。は、一定の圧力で、特定の量の物質に エネルギー (通常は熱)を供給してその状態を固体から液体に変化させることから生じる エンタルピー の変化です。たとえば、1 kgの氷を溶かすと( 広範囲の圧力 の下で0°Cで)、333




水比熱kj Kg 物理電磁學 電路工作紙一 Ynf




物質の三態 潜熱 高校物理 熱力学 熱量の保存2 物質の三態 融解熱 蒸発熱 授業 Youtube
高分子の融解熱が工業的に利用された例は聞かない が,蓄熱材料として実験段階で使用されたポリエチレン に関する研究報告18)がでている.融解熱は基礎的な物性 値であるため,科学的な観点から最大融解熱のチャンピ融解熱 (ゆうかいねつ)は一定の量の 物質 が 固体 から 液体 に 相転移 する時に必要な熱量( 潜熱 )である。 凝固熱 と等しい。 単位は J / g またはJ/ mol である。 ジュール については、主に kJ として用いることが多い。 氷 の融解熱は3336 kJ/kgである 。融解熱・蒸発熱は,普通,1気圧下において,1mol または1g あたりの熱エネルギー量で表す。 なお,気体から液体へ(凝結あるいは凝縮),液体から固体へ(凝固)にあたっては,それぞれ,蒸発熱,融解熱に等しい熱エネルギーを放出する。




高校化学 蒸発熱と昇華熱 映像授業のtry It トライイット
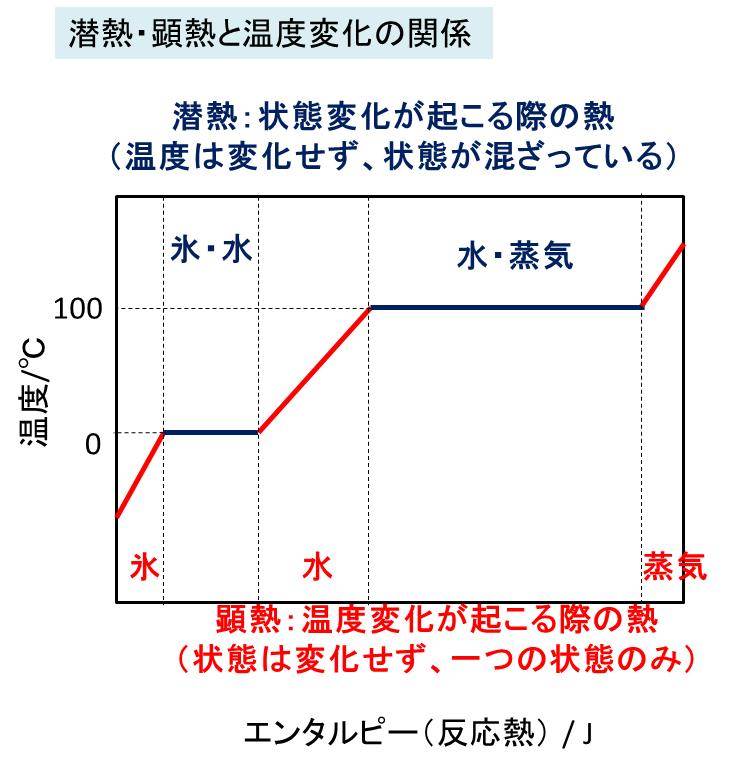



水の凝固熱 凝固エンタルピー の計算問題を解いてみよう 凝固熱と温度変化
添加し試作したノルマルパラフィンエマルションのDSC測定結果を示した。凝固、融解の 際の融解熱、凝固熱はそれぞれ-85kJ/ kg、85kJ/ kgであり、放熱、吸熱での特性に違い がないことも明らかとなった。 3.4 増粘剤の検討 ②融解熱 (ゆうかいねつ) ③溶解熱 (ようかいねつ) の3つです。 ①凝固点降下 (ぎょうこてんこうか) って何? 水は0度になると固体になり、 氷へ変化します。 また、冷凍庫のような0度よりも低いところにあると 常に氷のままでいられますが、相転移を含む定圧過程の熱 水の定圧比熱容量 ( )、融解エンタルピー、蒸発エンタルピーが以下の値であるとする。 定圧比熱容量 (氷) 210 J K −1 g −1 定圧比熱容量 (水) 4 J K −1 g −1 定圧比熱容量 (水蒸気) 186 J K −1 g −1 比融解エンタルピー



Introduction To Hydrological Cycle Koji Yamazaki Ir Image




蛋白软糖和冰淇凌奶蛋烘饼与融解热巧克力顶部在热板倾吐影视素材 视频包括有液体 熔化 装饰 甜甜
固体内を熱伝導で熱が移動する場合について考えてみる.図1 に示すように,単一の固 体内に2 つの等温面(isothermal plane) を考える.面積Aの二面の温度をそれぞれT1, T2 (T1 > T2) とし,その間隔を∆xとする.このとき,熱はそれぞれの等温面に垂直な方向融解温度、降温時の23℃の発熱ピークは溶融 状態から結晶化する降温結晶化温度(Tmc)で す。測定例では1st Runと2nd Runのピーク 温度は9℃異なりました。 一般的にポリマーの融解現象は熱履歴によ り変わるため、一度サンプルを完全に融解さこのとき1mol あたり502kJの熱 を放出する。エチルアルコールの凝固モルエントロピーを求めよ。 《-3164JK-1mol -1》 問4白金は1気圧,1772℃で融解して液体になる。このとき1mol あたり217kJの熱を吸収する。白金の融解モル




高校物理 潜熱 映像授業のtry It トライイット




融解熱 萌典
氷の融解熱(Ji) = 80cal/g = J/g 1gの水の温度を1℃上昇させるのに必要な熱量が1calである。融解熱は水の温度を80℃上昇させるエネルギーに匹敵し、かなり大きい。地上の全氷の融解熱も計算す7 日本熱物性学会研究分科会 「低温環境における熱物性の基礎と応用」 08/ 9/ 5 水溶液中の氷の融解潜熱の定義 氷の単位質量あたり ql ipf 8 日本熱物性学会研究分科会 「低温環境における熱物性の基礎と応用」 08/ 9/ 5 凝固点降下に伴う固液間の エンタルピー差の変化融解熱 ユウカイネツ heat of fusion 固体が融解して液体になるときに吸収する熱量をいい,融解の潜熱ともいう.固体1 g あるいは1 mol を基準にとる場合が多く,後者をとくにモル融解熱という.




水の昇華熱は51kjと決まっていないのですか Clear




第1回 熱と仕事 日本機械学会誌
るより融解によって壊れにくいことを示している。 3.3 融解過程に関する理論的取り扱い 雪片の融解過程に関係する熱は,外気から熱伝導で輸送される熱と,雪片表面で起こる水の相変 化に伴う潜熱融解 ユウカイ fusion, melting 溶融ともいう.固相にある物質が熱せられて液相になる変化をいう.分子論的な機構としては結晶の温度が高くなると分子の熱振動ははげしくなり,振動の振幅は漸次増大し,非調和的な振動になっていく.このような振動がある程度(分子間距離の10% 程度)以上に物質 温度 ℃ 融解熱 kJ/kg 亜鉛 4196 101 アルミニウム 6601 397 アンチモン 6307 165 アンモニア77 333 エチルアルコール




センター16物理基礎追試第1問 問3 水の比熱と融解熱 理科が好き Com




比熱 熱量 氷の融解のグラフ問題を解説 Youtube
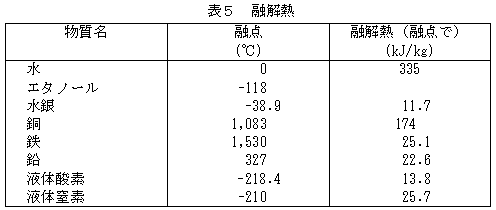
「融解熱(融解に必要な熱エネルギー)と凝固熱(凝固で余る熱エネルギー)とは等しい。」このような温度変化をもたらさない熱エネルギーのことを潜熱という。 表5 - 1 融点と融解熱 こ( ̄0 ̄)ん( ̄ー ̄)に( ̄  ̄)ち"<( ̄∇ ̄)>"わっはっは!!さて、固体,液体,気体の違いは、皆さんなら説明できるでしょう。が、念のために・・・・r( ω )まず、固体と液体,気体との最大の違いは、変形のしやすさでしょう。実際の物質は構成粒子からできていて、粒子間には隙間




酢酸ナトリウム三水和物を用いた 融解における温度変化の測定




高校化学 溶解熱と中和熱 映像授業のtry It トライイット




教えてください 分子量と融解熱と蒸発熱の使い方を教えてください Clear




ヤフオク マギ 同人 ジュダル シンドバッド Judal S




Entry Details For 融解熱 Yuukainetsu Tanoshii Japanese




2 9 潛熱和顯熱和蒸發熱 氣化熱
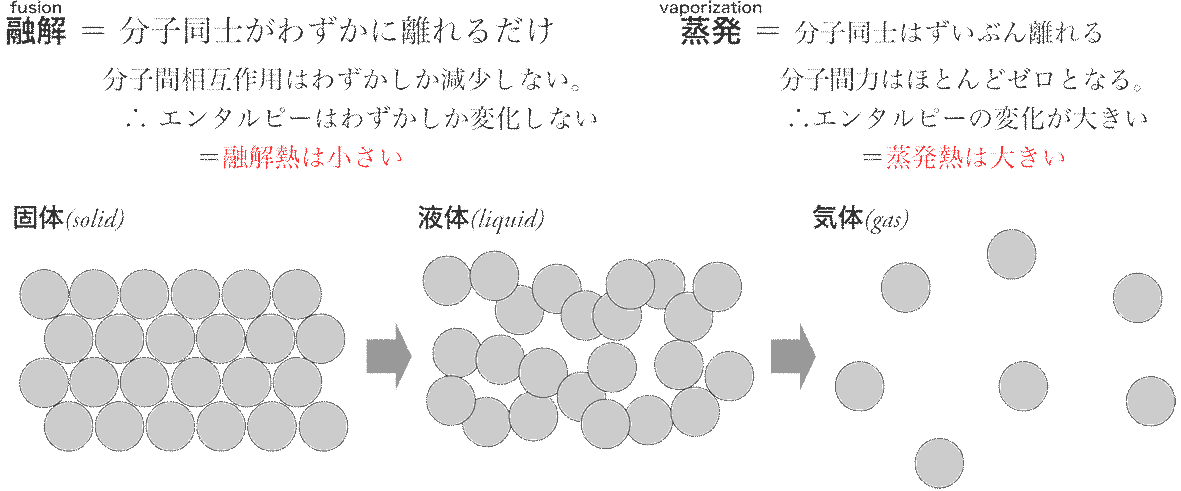



化学屋の呟き Ssブログ



なんとなくわかる高校化学 融解熱 蒸発熱




知识回顾什么是可逆过程和不可逆过程 克劳修斯等式 不等式热力学第二定律是什么 热力学第二定律如何表述 卡诺定理 Ppt




高校化学 物質の状態と平衡01 状態変化と熱 7分 Youtube



Www Clearize Co Jp Wp Content Uploads 10 615af3cbbbe05b8e2 Pdf



反応熱とは 吸熱反応 発熱反応 制御工学の基礎あれこれ



氷の融解熱と水の比熱の計算方法がわかりません 明日小テスト Yahoo 知恵袋




1 2 3 水の注目すべき特性 2 比熱容量 気化熱 融解熱 熱伝導率 水の話




理論 三態変化 受験 定期テストで高校化学を完全攻略




水の科学4 融解熱 蒸発熱が大きい Aqua Sphere




比熱heat Chchl




1g 90j 0 0g 66times1 Lihat Cara Penyelesaian Di Qanda




魔奇少年magi 辛巴達受裘辛融解熱 露天拍賣




どうしてこの様になるのかが分かりません どなたか教えて頂けませんか Clear



化学講座 第46回 凝固点降下 私立 国公立大学医学部に入ろう ドットコム
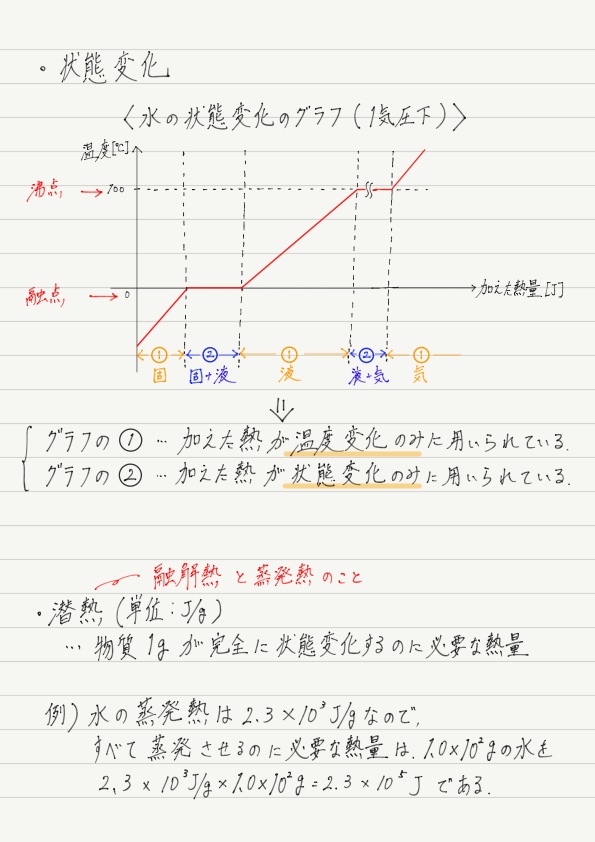



物質の状態変化と潜熱 高校物理をあきらめる前に 高校物理をあきらめる前に



Adoko 熱力学 物理基礎の熱力学




化学基礎を専攻する文系の人も必見 物質の三態 数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc



融解熱6 0kj Molが氷1molを融解するために6 0kjの熱が必 Yahoo 知恵袋




蛋白软糖和冰淇凌奶蛋烘饼与融解热巧克力顶部在热板倾吐影视素材 视频包括有液体 熔化 装饰 甜甜



1 2 3 水の注目すべき特性 2 比熱容量 気化熱 融解熱 熱伝導率 水の話




5分でわかる潜熱 身近な現象や技術は 理系学生ライターがわかりやすく解説 ページ 2 3 Study Z ドラゴン桜と学ぶwebマガジン
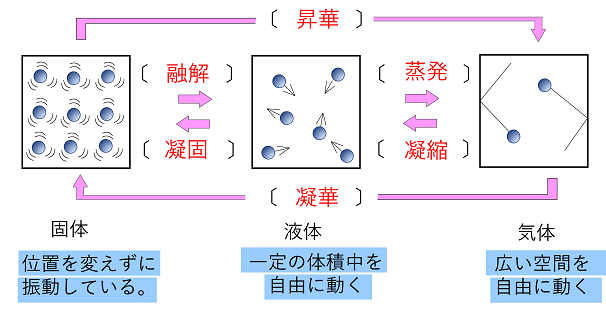



物質の三態と熱運動



高校化学 物質の状態 物質の三態と分子間力 Tekibo



受験化学 1 物質の三態と状態変化 みかみの参考書ブログ




Meme 涼感系列 妊婦帶size M L 腹圍 81 110cm 臀圍85 104 Cm Facebook




代購屋 同人誌 名偵探柯南 Fiore おうり 融解熱はまだ足りない 赤井秀一 安室透 露天拍賣
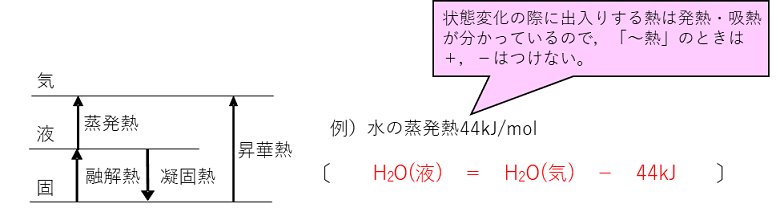



化学変化とエネルギー



Magicpoint Presentation Foils



ネギシの潜熱蓄熱材




物理基礎 力学06 比熱 融解熱 気化熱 蒸発熱 を利用した状態変化問題 熱量保存 高校物理 Youtube




高校物理 潜熱 練習編 映像授業のtry It トライイット




物質の状態変化 融解 凝固 と反応熱の関係を元塾講師が解説 Study Z ドラゴン桜と学ぶwebマガジン



なんとなくわかる高校化学 融解熱 蒸発熱
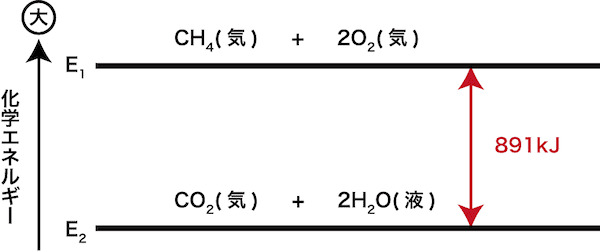



一覧 反応熱 燃焼熱 融解熱 解離エネルギーなど 総まとめ 化学のグルメ




反応熱の計算 生成熱 燃焼熱 溶解熱 中和熱 結合エネルギー 理系ラボ




水の昇華熱は51kjと決まっていないのですか Clear




ヤフオク マギ 同人 ジュダル シンドバッド Judal S




物理基礎 熱力学05 比熱 融解熱を利用した問題 熱量の保存 状態変化がキーポイント 高校物理 Youtube




2 で質問なんですが容器の比熱はずっと一定ということで合っていますか Clear




Lite版 危険物取扱者試験乙4 30日合格プログラム Lite版 危険物取扱者試験乙4 30日合格プログラム 下载 苹果好玩网



Http Ir Lib Cyut Edu Tw 8080 Bitstream 1 5 E6 Ba B6 E8 A3 E7 86 B1 E4 B9 8b E6 B8 Ac E9 87 8f Pdf




Jis K Testing Methods For Heat Of Transitions Of Plastics Pdf 文档分享网




溶解熱初中化學 溶液 溶質 溶劑 Qavhp




04熱とエネルギー 潜熱 Youtube




Jis K Testing Methods For Heat Of Transitions Of Plastics Pdf 文档分享网




融解と凝固とは E M Jobs




三年級自然教學 陳俊龍的教學檔案 準時完備精緻從容效能
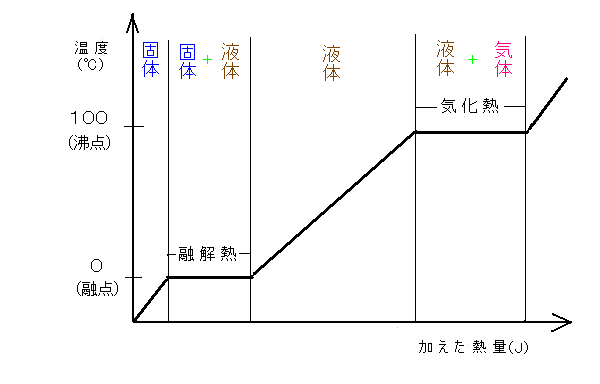



潜熱




高校物理 融解熱 映像授業のtry It トライイット
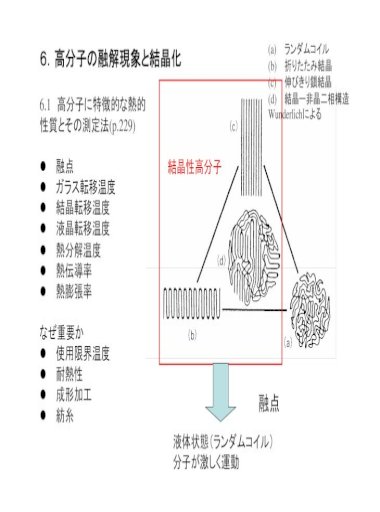



6 高分子の融解現象と結晶化 A ランダムコイル 義資料 高分子化学 融点 Tm




Fundamental Physics Laboratory For Engineer



こんなにすごい 氷のチカラ ブログ あゆむ整骨院



地球上の海水 氷 大気の熱容量 融解熱計算 Excelを用いた地球温暖化計算




Woa1 フィラー高充填高熱伝導性材料 およびその製造方法 並びに組成物 塗料液 および成形品 Google Patents




熱による材料の変化を試験したい 株式会社 クリアライズ



Adoko 熱力学 固体液体の熱力学




潜熱の種類と熱量 色と形で気象予報士




18追試 第1問 問5 融解熱とmol計算 化学がちょっとだけ好きな社労士
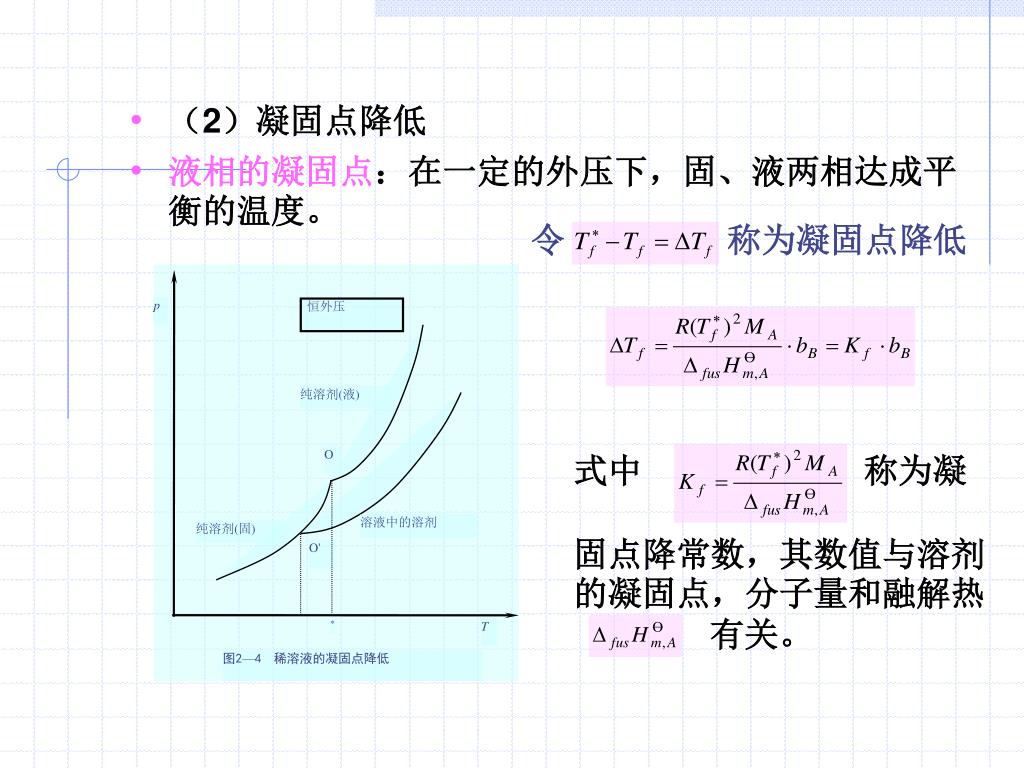



Ppt 第四章多组分系统热力学powerpoint Presentation Free Download Id




高校化学です 初歩的な質問ですみません Clear




高校 とってもやさしい化学 Amazon Es Libros




入試化学を語呂合わせで解く大学入試ゴロ化学




溶解度 溶解速度 Yakugaku Lab



融解熱について 氷が溶けて水になるような問題では 図のような様々な状況で融解 Yahoo 知恵袋




Tsukipro Burn To The Heat Of Fusion Mamoru Fujimura X Teru Takashi Eto Doujin Suruga Ya Com




改訂化学基礎 改訂化学 ダイジェスト版




の 2 から分からないのですが 答えしか載っていなくて解き方がわかりません 誰か教 Clear




高校化学 融解熱 映像授業のtry It トライイット



融解熱や蒸発熱のところで温度を加えているのに一定に保たれる理由は Yahoo 知恵袋




复习 一 质点运动学描写运动的三个物理量位矢速度曲线切向方向加速度切向加速度法向加速度 Ppt Download
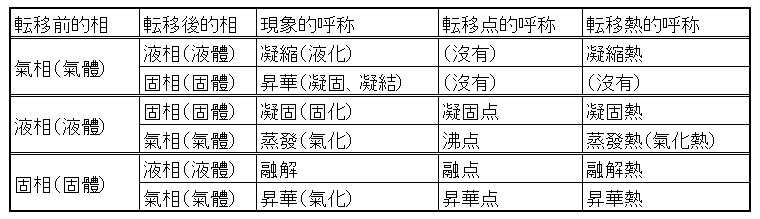



2 9 潛熱和顯熱和蒸發熱 氣化熱




融解熱と結晶化の違い 類似用語の違いを比較する 理科 21




2 で質問なんですが容器の比熱はずっと一定ということで合っていますか Clear



潜熱 物理化学を理解するために




融解熱とは サイエンスの人気 最新記事を集めました はてな




比熱 熱量 氷の融解のグラフ問題を解説 Youtube




物理基礎について教えて下さい 助けて下さい Okwave
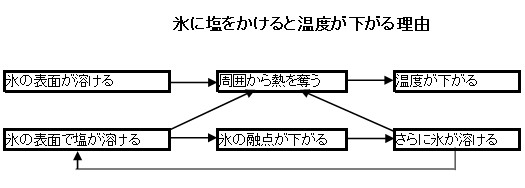



氷に塩をかけるとなぜ温度が下がるの なぜ早く溶けるの トレンドピックアップ




物質の三態と潜熱とは ぷち教養主義



0 件のコメント:
コメントを投稿